Mechanischer Reiz mit Folgen
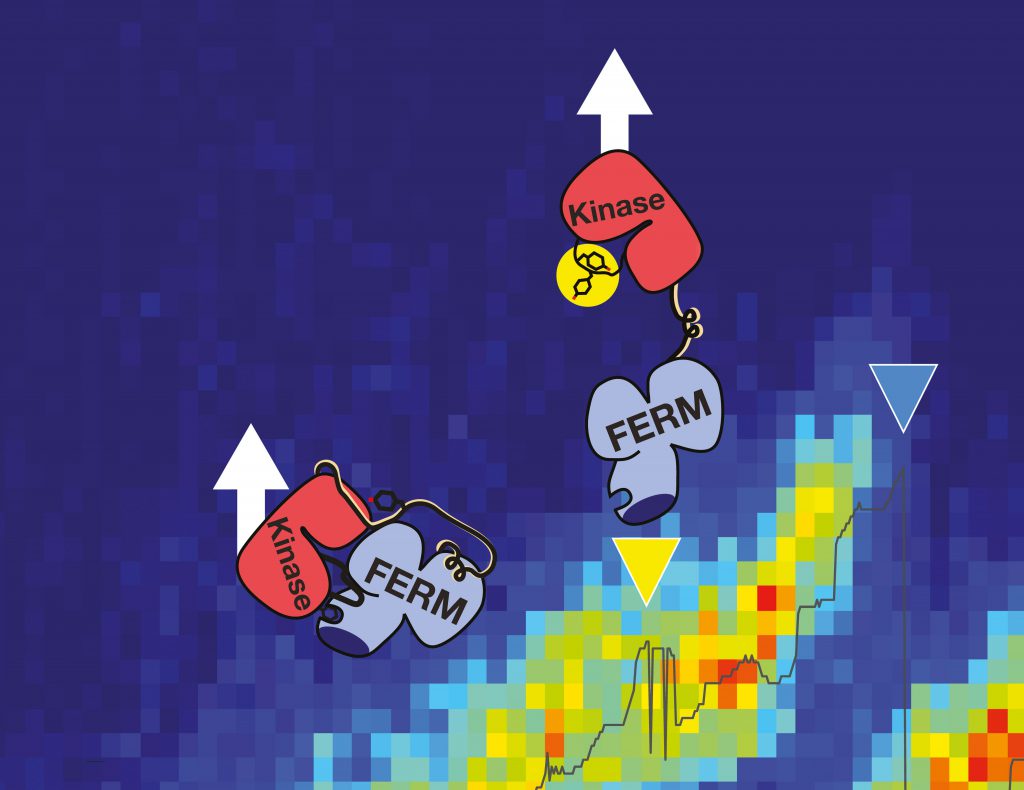
Tumorinvasion und Metastasierung gehören zu den großen Problemen im Kampf gegen Krebs. HITS-Forscher der Molecular Biomechanics Gruppe haben jetzt gemeinsam mit ihren Kooperationspartnern am CNIO Madrid und der LMU München den Aktivierungsprozess eines der beteiligten Schlüsselenzyme aufgeklärt. Daran kann die Entwicklung neuer Therapien ansetzen.
Um neue Wege zur Prävention von Tumor-Metastasen zu entwickeln, muss zunächst deren Entwicklungsprozess aufgeklärt werden. Die fokale Adhäsionskinase (FAK) ist ein Schlüsselenzym in der Signalkaskade, die zu Ausbreitung und Metastasierung von Tumoren führt. Dadurch wird sie zur idealen Zielstruktur für die Krebstherapie.
NIM-Wissenschaftler am Lehrstuhl von Professor Hermann Gaub an der Ludwig-Maximilians-Universität München haben zusammen mit ihren Kollaborationspartnern am Spanish National Cancer Research Centre in Madrid um Professor Daniel Lietha und am Heidelberger Institut für Theoretische Studien (HITS) um Professor Frauke Gräter einen Weg der Kraft-basierten Aktivierung der FAK nachgewiesen und in den Proceedings of the National Academy of Sciences of the United States of America publiziert.
Was ist der Auslöser?
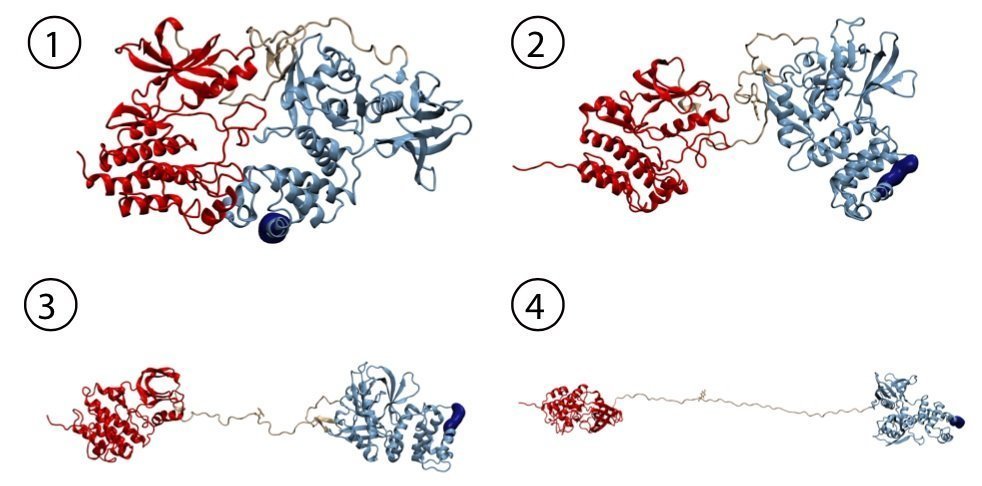
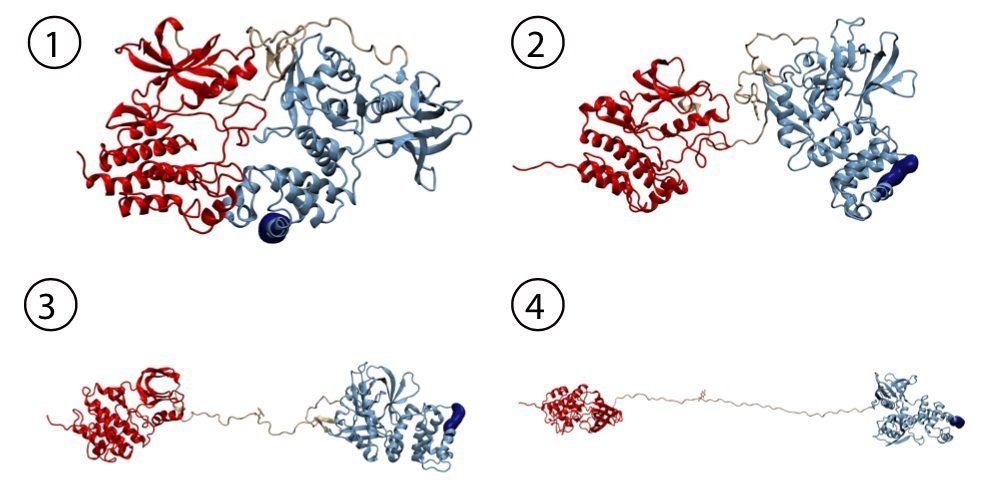
Als Signalprotein reguliert die FAK entscheidende Prozesse einer Zelle: Adhäsion, Migration und Zelltod. Die Kinasekomplexe liegen auf der Innenseite der Zellwand als Teil der sogenannten fokalen Adhäsionsstellen. Diese sind sozusagen die Füße der Zelle. „Im inaktiven Zustand ist die fokale Adhäsionskinase auto-inhibiert, das heißt das aktive Zentrum des Enzyms ist unzugänglich, geschützt durch eine Art Proteindeckel”, erklärt Magnus Bauer, Erstautor der Publikation und NIM-GP Doktorand an der LMU. „Unser Ziel war es herauszufinden, ob mechanische Kräfte diesen Deckel öffnen können und damit die Aktivierung dieses Schlüsselakteurs auslösen.“ Dies ist von besonderem Interesse, da die aktivierte FAK auch die Adhäsion an Tumorgewebe und generell die extrazelluläre Matrix vermittelt – eine Voraussetzung für Tumorinvasion und Metastasierung. Außerdem führt die Überexpression der FAK, wie man sie in den meisten Tumorzellen findet, zur Verhinderung des natürlichen Zelltods und der Abregulation des Tumorsuppressor-Gens p53.
Bindung mit Folgen
Das mechanische Umfeld einer Zelle beeinflusst ihr Verhalten. Die fokale Adhäsionskinase agiert als Sensor für Veränderungen, sowohl im extrazellulären, als auch im intrazellulären Gefüge. „In Einzelmolekül-Rasterkraftmikroskopie-Messungen und Molekulardynamiksimulationen konnten wir die Öffnung des inhibitorischen Komplexes unter mechanischer Belastung nachweisen, und damit indirekt ihre Aktivierung durch Kraft“, beschreibt der Physiker Bauer die experimentelle Herangehensweise in München. Das Team von Frauke Gräter in Heidelberg simulierte diesen Prozess mithilfe von High Performance Computern für eine vollständige dynamische Ansicht. „Wir haben erfolgreich die wichtigen Schritte der FAK Aktivierung dargestellt und konnten zeigen, dass FAK nicht nur durch Kraft aktiviert wird, sondern diese Aktivität auch lange beibehalten kann, selbst wenn es sehr langgestreckt wird“, erklärt Frauke Gräter. In Zellen wird die mechanische Aktivierung durch die Belastung von Zytoskelett und extrazellulärer Matrix ausgelöst. „Mit der FAK scheinen wir das erste Nicht-Muskelenzym gefunden zu haben, das direkt durch mechanische Kraft aktiviert wird“, betont Bauer. „Überträgt man unsere Ergebnisse auf ein zelluläres System, dann könnte die Übersetzung physiologischer Zugkräfte in biochemische Signale ein Weg sein, die Migration von Tumorzellen auszulösen.“ Diese fundamentalen Erkenntnisse über die Mechanismen eines Schlüsselenzyms für die Metastasierung von Tumoren eröffnen neue Möglichkeiten für zukünftige Krebstherapien.
Publikation:
Structural and mechanistic insights into mechanoactivation of Focal Adhesion Kinase. Bauer MS, Baumann F, Daday C, Redondo P, Durner E, Jobst MA, Milles LF, Mercadante D, Pippig DA, Gaub HE, Gräter F, Lietha D. PNAS, 2019, doi 10.1073/pnas.1820567116.
Wissenschaftliche Kontakte:
Prof. Dr. Hermann Gaub
Biophysics and Molecular Materials
Ludwig-Maximilians-Universität
Amalienstraße 54
D – 80799 München
Tel.: +49 (0)89 – 2180 3172
E-Mail: gaub@physik.uni-muenchen.de
Daniel Lietha, PhD
Cell Signaling and Adhesion Group
Structural and Chemical Biology
Biological Research Center (CIB-CSIC)
Calle Ramiro de Maeztu 9
E – 28040 Madrid
Spanien
Tel.: +34 (0)91 837 3112
E-Mail: daniel.lietha@cib.csic.es
Prof. Dr. Frauke Gräter
Molecular Biomechanics
Heidelberger Institut für Theoretische Studien (HITS)
Interdisciplinary Center for Scientific Computing (IWR), Heidelberg University
Schloss-Wolfsbrunnenweg 35
D – 69118 Heidelberg
Tel.: +49 6221 – 533 267
E-Mail: frauke.graeter@h-its.org
Über das HITS
Das HITS (Heidelberger Institut für Theoretische Studien) wurde 2010 von dem Physiker und SAP-Mitbegründer Klaus Tschira (1940-2015) und der Klaus Tschira Stiftung als privates, gemeinnütziges Forschungsinstitut gegründet. Es betreibt Grundlagenforschung in den Naturwissenschaften, der Mathematik und der Informatik. Zu den Hauptforschungsrichtungen zählen komplexe Simulationen auf verschiedenen Skalen, Datenwissenschaft und -analyse sowie die Entwicklung rechnergestützter Tools für die Forschung. Die Anwendungsfelder reichen von der Molekularbiologie bis zur Astrophysik. Ein wesentliches Merkmal des Instituts ist die Interdisziplinarität, die in zahlreichen gruppen- und disziplinübergreifenden Projekten umgesetzt wird. Die Grundfinanzierung des HITS wird von der Klaus Tschira Stiftung bereitgestellt.